ידע בהגדרות בפיזיקה הוא גורם מפתח לפתרון מוצלח של בעיות פיזיקליות שונות. במאמר, נשקול מה הכוונה בתהליכים איזובריים, איזוחוריים, איזותרמיים ואדיאבטיים עבור מערכת גז אידיאלית.
גז אידיאלי והמשוואה שלו
לפני שנמשיך לתיאור של תהליכים איזובריים, איזוחוריים ואיזותרמיים, הבה נבחן מהו גז אידיאלי. לפי הגדרה זו בפיזיקה הם מחשיבים מערכת המורכבת ממספר עצום של חלקיקים חסרי מימד ולא מקיימים אינטראקציה שנעים במהירויות גבוהות לכל הכיוונים. למעשה, אנו מדברים על מצב מצטבר גזי של חומר, שבו המרחקים בין אטומים למולקולות עולים בהרבה על גודלם ושבו מוזנחת האנרגיה הפוטנציאלית של אינטראקציה של חלקיקים בשל הקטנות שלה, בהשוואה לאנרגיה הקינטית.
מצבו של גז אידיאלי הוא מכלול הפרמטרים התרמודינמיים שלו. העיקריים שבהם הם טמפרטורה, נפח ולחץ. נסמן אותם באותיות T, V ו-P, בהתאמה. בשנות ה-30 של המאה ה- XIXקלפיירון (מדען צרפתי) רשם לראשונה משוואה המשלבת את הפרמטרים התרמודינמיים המצוינים בתוך שוויון אחד. זה נראה כמו:
PV=nRT,
כאשר n ו-R הם כמות החומרים וקבוע הגז, בהתאמה.
מהם תהליכי איזו בגזים?
כפי שרבים שמו לב, תהליכים איזובריים, איזוחוריים ואיזותרמיים משתמשים באותה תחילית "iso" בשמותיהם. המשמעות היא שוויון של פרמטר תרמודינמי אחד במהלך כל התהליך, בעוד שאר הפרמטרים משתנים. לדוגמה, תהליך איזותרמי מצביע על כך שכתוצאה מכך, הטמפרטורה המוחלטת של המערכת נשמרת קבועה, בעוד שתהליך איזוחורי מצביע על נפח קבוע.
Isoprocess נוחים למחקר, שכן תיקון אחד מהפרמטרים התרמודינמיים מוביל לפישוט המשוואה הכללית של מצב הגז. חשוב לציין שחוקי הגז עבור כל תהליכי האיזו הללו התגלו בניסוי. הניתוח שלהם אפשר לקלפיירון להשיג את המשוואה האוניברסלית המופחתת.
תהליכים איזובריים, איזוחוריים ואיזוטרמיים
החוק הראשון התגלה לתהליך איזותרמי בגז אידיאלי. עכשיו זה נקרא חוק בויל-מריוט. מכיוון ש-T לא משתנה, משוואת המצב מרמזת על השוויון:
PV=const.
במילים אחרות, כל שינוי בלחץ במערכת מוביל לשינוי ביחס הפוך בנפח שלה, אם טמפרטורת הגז נשמרת קבועה. הגרף של הפונקציה P(V) הואהיפרבולה.
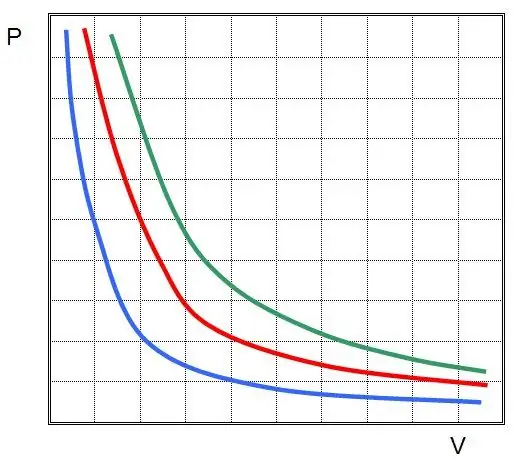
תהליך איזוברי - זהו שינוי במצב המערכת, בו הלחץ נשאר קבוע. לאחר שנקבע את הערך של P במשוואת קלפיירון, נקבל את החוק הבא:
V/T=const.
שוויון זה נושא את שמו של הפיזיקאי הצרפתי ז'אק שארל, שקיבל אותו בסוף המאה ה-18. האיזובר (ייצוג גרפי של הפונקציה V(T)) נראה כמו קו ישר. ככל שיש יותר לחץ במערכת, כך הקו הזה עולה מהר יותר.
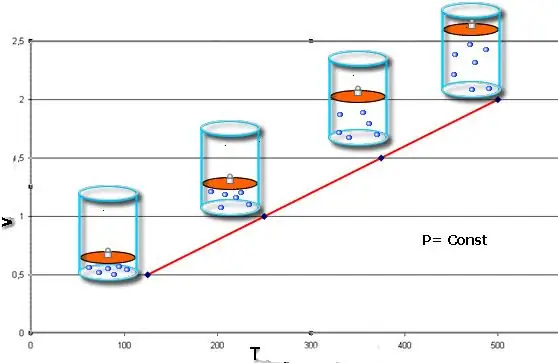
התהליך האיזוברי קל ליישום אם הגז מחומם מתחת לבוכנה. המולקולות של האחרונים מגבירות את מהירותן (אנרגיה קינטית), יוצרות לחץ גבוה יותר על הבוכנה, מה שמוביל להתרחבות הגז ולשמירה על ערך קבוע של P.
לבסוף, האיזו-תהליך השלישי הוא איזוכורי. הוא פועל בנפח קבוע. ממשוואת המצב נקבל את השוויון התואם:
P/T=const.
זה ידוע בקרב הפיזיקאים כחוק גיי-לוסאק. המידתיות הישירה בין לחץ לטמפרטורה מוחלטת מצביעה על כך שהגרף של התהליך האיזוחורי, כמו הגרף של האיזוברי, הוא קו ישר עם שיפוע חיובי.
חשוב להבין שכל תהליכי האיזו מתרחשים במערכות סגורות, כלומר, הערך של n נשמר במהלך המהלך שלהם.
תהליך אדיאבטי
תהליך זה אינו שייך לקטגוריית "iso", מכיוון שכל שלושת הפרמטרים התרמודינמיים משתנים במהלך המעבר שלו. אדיאבטינקרא המעבר בין שני מצבים של המערכת, שבהם היא אינה מחליפה חום עם הסביבה. כך, הרחבת המערכת מתבצעת עקב מאגרי האנרגיה הפנימיים שלה, מה שמביא לירידה משמעותית בלחץ ובטמפרטורה המוחלטת בה.
תהליך אדיאבטי לגז אידיאלי מתואר על ידי משוואות פואסון. אחד מהם מוצג להלן:
PVγ=const,
כאשר γ הוא היחס בין יכולות החום בלחץ קבוע ובנפח קבוע.
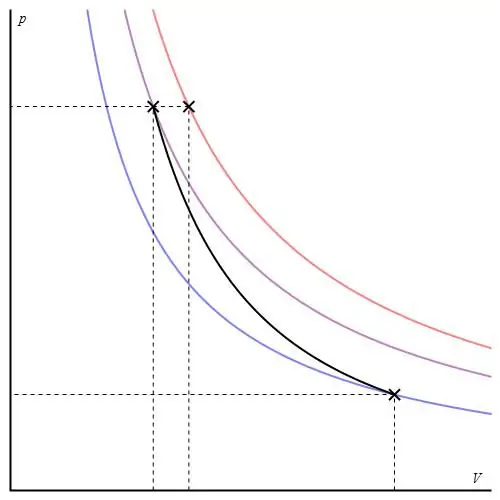
הגרף האדיאבטי שונה מגרף התהליך האיזוחורי ומהגרף האיזוברי, אך הוא דומה להיפרבולה (איזותרמית). האדיאבט בצירי P-V מתנהג בצורה חדה יותר מהאיזותרמי.






