בתרמודינמיקה, כאשר לומדים מעברים מהמצב הראשוני לסופי של מערכת, חשוב לדעת את ההשפעה התרמית של התהליך. הרעיון של קיבולת חום קשור קשר הדוק להשפעה זו. במאמר זה נשקול את השאלה מה הכוונה בקיבולת החום האיזוכורית של גז.
גז אידיאלי
גז אידיאלי הוא גז שחלקיקיו נחשבים לנקודות חומריות, כלומר אין להם ממדים, אלא בעלי מסה, ושכל האנרגיה הפנימית בו מורכבת אך ורק מהאנרגיה הקינטית של תנועת מולקולות ואטומים.
כל גז אמיתי, באופן אידיאלי, לעולם לא יספק את המודל המתואר, שכן לחלקיקים שלו עדיין יש מימדים ליניאריים והם מקיימים אינטראקציה זה עם זה באמצעות קשרים חלשים של ואן דר ואלס או קשרים כימיים מסוג אחר. עם זאת, בלחצים נמוכים ובטמפרטורות גבוהות, המרחקים בין מולקולות גדולים, והאנרגיה הקינטית שלהן עולה על האנרגיה הפוטנציאלית בעשרות מונים. כל זה מאפשר ליישם ברמת דיוק גבוהה את הדגם האידיאלי לגזים אמיתיים.
אנרגיה פנימית של גז
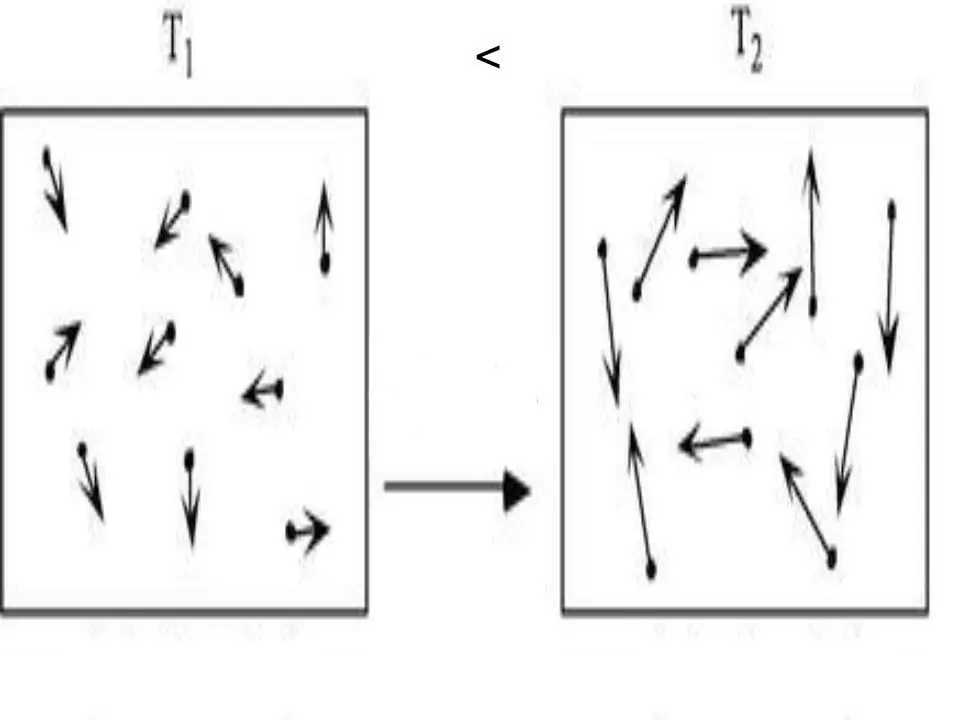
האנרגיה הפנימית של כל מערכת היא מאפיין פיזי, ששווה לסכום האנרגיה הפוטנציאלית והקינטית. מכיוון שניתן להזניח אנרגיה פוטנציאלית בגזים אידיאליים, נוכל לכתוב עבורם את השוויון:
U=Ek.
היכן Ek היא האנרגיה של המערכת הקינטית. באמצעות התיאוריה הקינטית המולקולרית ויישום משוואת המדינה האוניברסלית קלפיירון-מנדלייב, לא קשה להשיג ביטוי ל-U. זה כתוב להלן:
U=z/2nRT.
כאן T, R ו-n הם הטמפרטורה המוחלטת, קבוע הגז וכמות החומר, בהתאמה. ערך z הוא מספר שלם המציין את מספר דרגות החופש שיש למולקולת גז.
קיבולת חום איזוברית ואיזוכורית
בפיזיקה, קיבולת חום היא כמות החום שיש לספק למערכת הנבדקת כדי לחמם אותה בקלווין אחד. ההגדרה ההפוכה נכונה גם היא, כלומר, קיבולת החום היא כמות החום שהמערכת משחררת כאשר היא מתקררת בקלווין אחד.
הדרך הקלה ביותר למערכת היא לקבוע את קיבולת החום האיזוכורית. זה מובן כיכולת החום בנפח קבוע. מכיוון שהמערכת אינה מבצעת עבודה בתנאים כאלה, כל האנרגיה מושקעת בהגדלת מאגרי האנרגיה הפנימיים. הבה נסמן את קיבולת החום האיזוכורית בסמל CV, ואז נוכל לכתוב:
dU=CVdT.
כלומר, השינוי באנרגיה הפנימיתהמערכת עומדת ביחס ישר לשינוי בטמפרטורה שלה. אם נשווה את הביטוי הזה עם השוויון שנכתב בפסקה הקודמת, אז נגיע לנוסחה של CV בגז אידיאלי:
СV=z/2nR.
ערך זה לא נוח לשימוש בפועל, מכיוון שהוא תלוי בכמות החומר במערכת. לכן, הוצג הרעיון של קיבולת חום איזוחורית ספציפית, כלומר, ערך המחושב לכל מול גז אחד או לכל ק ג. הבה נסמן את הערך הראשון בסמל CV, השני - בסמל CV m. עבורם, אתה יכול לכתוב את הנוסחאות הבאות:
CV=z/2R;
CVm=z/2R/M.
כאן M היא המסה הטוחנת.
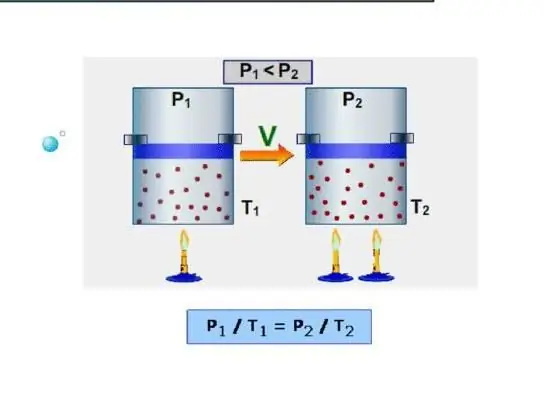
איזוברית היא קיבולת החום תוך שמירה על לחץ קבוע במערכת. דוגמה לתהליך כזה היא התפשטות הגז בצילינדר מתחת לבוכנה כאשר הוא מחומם. בניגוד לתהליך האיזוכורי, במהלך התהליך האיזוברי, החום המסופק למערכת מושקע להגברת האנרגיה הפנימית ולביצוע עבודה מכנית, כלומר:
H=dU + PdV.
האנטלפיה של תהליך איזובארי היא תוצר של קיבולת החום האיזוברי והשינוי בטמפרטורה במערכת, כלומר:
H=CPdT.
אם ניקח בחשבון את ההתפשטות בלחץ קבוע של 1 מול גז, אז החוק הראשון של התרמודינמיקה ייכתב כך:
CPdT=CV dT + RdT.
האיבר האחרון מתקבל מהמשוואהקלפיירון-מנדלייב. מתוך שוויון זה נובע הקשר בין יכולות חום איזובריות ואיזוכוריות:
CP=CV + R.
עבור גז אידיאלי, קיבולת החום המולארית הספציפית בלחץ קבוע גדולה תמיד מהמאפיין האיזוכורי המקביל ב-R=8, 314 J/(molK).
דרגות חופש של מולקולות וקיבולת חום
בוא נכתוב שוב את הנוסחה עבור קיבולת החום האיזוכורית הטוחנית הספציפית:
CV=z/2R.
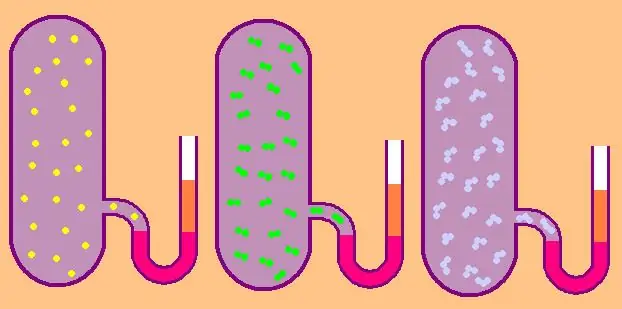
במקרה של גז מונוטומי, הערך z=3, שכן אטומים בחלל יכולים לנוע רק בשלושה כיוונים בלתי תלויים.
אם אנחנו מדברים על גז המורכב ממולקולות דיאטומיות, למשל, חמצן O2 או מימן H2, אז, בנוסף לתנועה תרגום, מולקולות אלו עדיין יכולות להסתובב סביב שני צירים מאונכים זה לזה, כלומר, z יהיה שווה ל-5.
למולקולות מורכבות יותר, השתמש ב-z=6. כדי לקבוע CV






